Os principais erros da fase pré-analítica de exames laboratoriais
The main errors of the pre-analytical phase of laboratory exams
Raquel Gomes de Assis Molina de Oliveira1, Giselle Aparecida Fagundes Silva2
1 Biomédica / Universidade do Grande Rio. Duque de Caxias, RJ, Brasil.
2 Doutorado/ Universidade do Grande Rio. Duque de Caxias, RJ, Brasil.
Recebido em 22/12/2020
Aprovado em 17/03/2022
DOI: 10.21877/2448-3877.202202089
INTRODUÇÃO
A medicina laboratorial desempenha um papel de suma importância na área da saúde, onde disponibilizam serviços de análises, estudos de materiais biológicos e diversas outras atividades voltadas para a realização de exames complementares, que possuem finalidades diagnósticas, prognósticas, de prevenção e acompanhamento terapêutico, de forma que os resultados fornecidos através deles detêm uma grande influência em relação às decisões clínicas na assistência à saúde.(1)
Aproximadamente 70% dos diagnósticos são concluídos com base nos resultados das análises laboratoriais. Desta forma, é necessário que a medicina diagnóstica preze pela emissão de resultados confiáveis, gerando assim um serviço de saúde eficaz e seguro ao médico e ao paciente, pois além do diagnóstico influenciaria também as decisões médicas quanto à escolha de melhores estratégias terapêuticas e cuidados clínicos, como prescrição de medicamentos, internação, alta hospitalar, entre outras decisões assistenciais.(2-4)
Logo, os laboratórios clínicos possuem uma grande responsabilidade em relação às suas funções, constituindo inúmeras etapas que vão desde o cadastramento do paciente até a emissão e entrega dos laudos, que devem ser realizados com precisão para que se obtenham resultados coerentes e fidedignos, sendo estes condizentes com a realidade clínica do paciente. Isso é necessário e de extrema importância para que o médico possa se basear em seus resultados, a fim de que haja a correta e a melhor tomada de decisão clínica em relação ao paciente.(5)
Fases de realização das análises laboratoriais
A realização de exames e testes dentro de um laboratório está dividida em três fases fundamentais, sendo elas: fase pré-analítica, analítica e pós-analítica. A fase pré-analítica envolve a indicação e solicitação do exame, cadastro do paciente, transmissão correta das instruções de preparo ao paciente (que são específicas para cada tipo de exame), coleta, identificação, armazenamento, acondicionamento, transporte, recebimento e análise dos padrões de aceitação e rejeição das amostras biológicas. Desta forma a fase pré-analítica une todas as etapas necessárias que antecedem a fase analítica.(6)
A fase analítica consiste na operação de variados métodos para realização da análise do material biológico. Nesta fase são utilizados diversos equipamentos que irão auxiliar e executar as análises dos ensaios, por isso ela se torna uma fase mais automatizada, que requer um controle de qualidade e calibração de equipamentos, assim como a preservação dos reagentes utilizados nestes, a fim de se obter resultados precisos dos analitos.(7)
E, por fim, a fase pós-analítica, que se inicia a partir da obtenção dos resultados quantitativos e qualitativos das análises das amostras biológicas, que dará origem à liberação do laudo, seguida pela avaliação do médico, que irá emitir o diagnóstico e tomar as decisões necessárias mediante aos resultados que foram estabelecidos.(8)
Contudo, existe a possibilidade de ocorrerem erros durante a execução destas fases, que podem afetar os seus resultados. A Figura 1 mostra as frequências dos erros nas três fases citadas anteriormente, segundo o estudo de Ambachew et al.(9) Nesta, é possível observar que 68% dos erros laboratoriais ocorrem na fase pré-analítica. Estes dados revelam a importância de se enfatizar a fase pré-analítica, já que esta tem se destacado e tem sido apontada em várias pesquisas pela sua concentração de altas taxas de erros laboratoriais. Isto porque um dos motivos é o fato de os laboratórios não conseguirem ter um controle sobre algumas das atividades ali executadas, e é sobre ela que irá se tratar este estudo.(4,9,10)
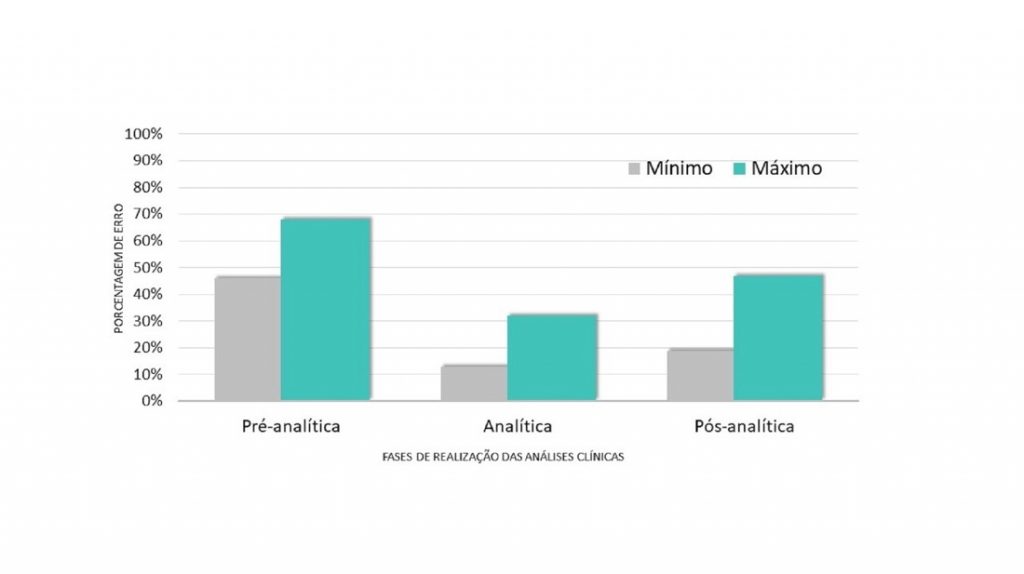
Figura 1
Comparação das porcentagens de erros entre as fases de realização das análises laboratoriais.
Fonte: Ambachew et al., 2018(9)
Fatores que influenciam os erros
Existem muitas pessoas envolvidas na realização da fase pré-analítica: paciente, médico, flebotomista e demais profissionais encarregados do armazenamento, transporte do material biológico e cadastramento do paciente. A ação destes dificulta a administração do laboratório em relação às atividades executadas, justamente por causa do elevado número de pessoas com diferentes graus de formação na área de saúde, ligados a realização das etapas desta fase.(5)
Um ponto que contribui para que haja essa grande quantidade de profissionais associados à fase pré-analítica está relacionado ao fato de a maioria dos processos não serem automatizados, como na fase analítica, o que torna essa fase mais vulnerável, pois quanto maior o número de pessoas envolvidas em um processo, maiores são as probabilidades de erros. Esta situação pode ser ainda mais difícil de controlar quando estas etapas são realizadas fora do ambiente laboratorial.(8)
Os termos “fase pré-pré-analítica e fase pós-pós-analítica” têm sido utilizados para designar as etapas de realização de exames que não dependem do laboratório, como por exemplo: a decisão médica sobre a escolha dos exames que são mais indicados mediante uma hipótese diagnóstica e a prescrição destes, o preparo do paciente para determinado exame, coleta, identificação das amostras, preservação, transporte e recepção do material biológico na fase pré-pré-analítica, e a interpretação do laudo feita pelo médico na fase pós-pós-analítica.(11)
As variáveis pré-analíticas têm grande impacto sobre os resultados dos exames laboratoriais, que podem promover interpretações errôneas. Por isso, informações relevantes sobre o paciente, como idade, gênero, variação cronobiológica, jejum, prática de atividades físicas, uso de medicamentos, tabagismo, etilismo, gestação, doenças ou lesões preexistentes, deverão ser consideradas, pois podem influenciar e comprometer os resultados dos exames, fazendo-se necessário o conhecimento destes dados na fase pré-analítica e pós-analítica, para avaliação dos resultados que forem obtidos.(12)
Desta forma, as altas taxas de erros pré-analíticos estão associadas à complexidade dos processos envolvidos, à limitada automação e padronização dos serviços e à participação de diversas pessoas na fase pré-analítica, tornando-a vulnerável e gerando não conformidades nos processos desta etapa. A não conformidade é a ocorrência de um procedimento não padronizado, ou seja, é o não cumprimento de um requisito, que pode levar a resultados enganosos, por isso cada laboratório desenvolve métodos próprios para lidar com estes obstáculos.(10)
Um erro pode provocar falsos positivos ou falsos negativos e interferir na decisão médica quanto ao quadro clínico e diagnóstico do paciente, que eventualmente em alguns casos terá que refazer o exame, gerando assim gastos e atrasos no diagnóstico ou até mesmo danos à saúde do paciente.(13)
Os laboratórios clínicos e sua equipe multidisciplinar necessitam seguir as normas, regulamentações e as recomendações das boas práticas laboratoriais, a fim de minimizar ou evitar possíveis erros, e não influenciar de alguma maneira os resultados dos exames. Além disso, fazer a adoção de programas de gestão da qualidade através dos indicadores de qualidade é de extrema importância, pois estes irão realizar um mapeamento dos processos laboratoriais para identificar, qualificar e quantificar falhas que possam existir, permitindo assim que medidas de prevenção e correção sejam colocadas em prática.(11)
De igual modo, a busca pela acreditação e certificação de um laboratório é primordial para promover segurança, responsabilidade, ética profissional, eficiência e oferecer serviços de alta qualidade. Colocar em prática este processo irá viabilizar a padronização das atividades realizadas no âmbito laboratorial e gerar a busca pela melhoria contínua dos serviços de saúde.(14)
O alto percentual de erros cometidos na fase pré-analítica destaca-se quando comparado com os percentuais de erros das outras duas fases de realização de exames laboratoriais. Além disso, um pequeno erro cometido nesta fase é crucial para comprometer as próximas etapas e principalmente os resultados dos exames.(6)
Desta forma, estas foram as questões motivadoras para a criação deste trabalho, pois é necessário primeiramente conhecer os erros e suas origens, para então possibilitar o desenvolvimento de soluções, a fim de reduzir a taxa de ocorrência desses erros e desta forma melhorar a qualidade dos serviços laboratoriais.
Portanto, o presente estudo tem como objetivo identificar os principais erros que estão vinculados à fase pré-analítica, assim como os impactos que esses erros podem causar, baseando-se na literatura científica. O intuito é mostrar a relevância deste assunto e as questões preponderantes que devem ser evitadas durante uma rotina laboratorial, podendo este ser usado eventualmente como fonte de dados para estudantes ou profissionais da área da saúde, a fim de gerar discussões, estudos, levantamento de dados, busca por soluções e principalmente reavaliação das condutas durante a realização dos ensaios.
MATERIAL E MÉTODOS
Para a elaboração desta revisão de literatura, foram utilizados como base artigos científicos obtidos através dos bancos de dados eletrônicos e revistas científicas, sendo estes: PubMed (que utiliza artigos fornecidos pelo MEDLINE), Scientific Electronic Library Online (SciELO), Scientific Electronic Library Online Saúde Pública (SciELOSP), Literatura Latino-Americana e do Caribe em Ciências da Saúde (LILACS), ScienceDirect (Elsevier), Google Acadêmico e a Revista Brasileira de Análises Clínicas (RBAC). As palavras-chaves utilizadas na busca dos artigos nestes bancos de dados são: fase pré-analítica, erros pré-analíticos, erro laboratorial e análises clínicas.
Durante a pesquisa, foram selecionados artigos publicados nos idiomas português, inglês ou espanhol, entre o período de 2011 a 2020, com base no título e na leitura do resumo. Após o levantamento bibliográfico, cerca de 80 artigos foram coletados, e deste total 29 estudos foram selecionados para embasar o presente trabalho. As tabelas e figuras presentes nesta revisão foram desenvolvidas nos programas do Microsoft Excel e do Microsoft Word, utilizados para compilar os dados com base na literatura, reunindo apenas informações relevantes e inerentes ao objetivo deste estudo.
RESULTADOS
O baixo desempenho laboratorial pode causar erros, e consequentemente o aumento dos custos de assistência médica, atrasos no diagnóstico e tratamento, ou até mesmo diagnóstico incorreto e tratamento inadequado e, com isso, a diminuição da satisfação do paciente. Os erros podem ocorrer em qualquer parte do processo, todavia, a fase pré-analítica tem apresentado altos índices de erros, destacando-se quando comparada às outras duas fases do processo de realização dos testes. O impacto causado pelo erro pré-analítico pode gerar danos como os citados anteriormente, assim como a rejeição de amostras que leva à realização de novas coletas.(9)
Um dado importante é relatado no estudo de Fernandes e Oliveira,(6) onde a pesquisa foi realizada em um laboratório privado na cidade de Maringá-PR, Brasil, que mostrou que 1.274 testes laboratoriais receberam novas ordens de coleta, devido a erros laboratoriais que provocaram a rejeição das amostras biológicas. Com isso, a fase pré-analítica está representando a maior taxa de pedidos de nova coleta (70,8%), seguida pela fase pós-analítica (27,79%) e por fim a fase analítica com uma pequena taxa (1,41%), conforme mostra a Figura 2.(6)
Há pouco tempo, um estudo prospectivo desenvolvido por Ashakiran et al.(15) já demonstrava que a fase pré-analítica é responsável pela maior parte dos erros registrados, já que estes atingiram uma margem de 44,7% de erros pré-analíticos por dia. No estudo, foram monitorados a frequência e os tipos de erros, através da análise das amostras de sangue venoso. A Tabela 1 mostra os erros pré-analíticos que foram documentados e sua distribuição percentual no período de três meses do estudo.(15)
Ratificando o estudo de Ashakiran et al.,(15) Guimarães et al. (16) avaliaram os dados obtidos através da análise de rejeição de amostras de sangue, assim como as solicitações de novas coletas de sangue diárias, no Hospital de Clínicas de Porto Alegre. O estudo mostrou que do total de 77.051 amostras de sangue, 441 (0,57%) amostras foram rejeitadas por serem consideradas como inadequadas para a realização de exames, por possuir algum tipo de erro pré-analítico. A Tabela 2 mostra os motivos que levaram a rejeição das amostras, assim como as frequências de suas ocorrências. Amostras coaguladas e hemolisadas, juntamente com volume insuficiente de amostra foram as causas mais frequentes na rejeição dos espécimes.(16)
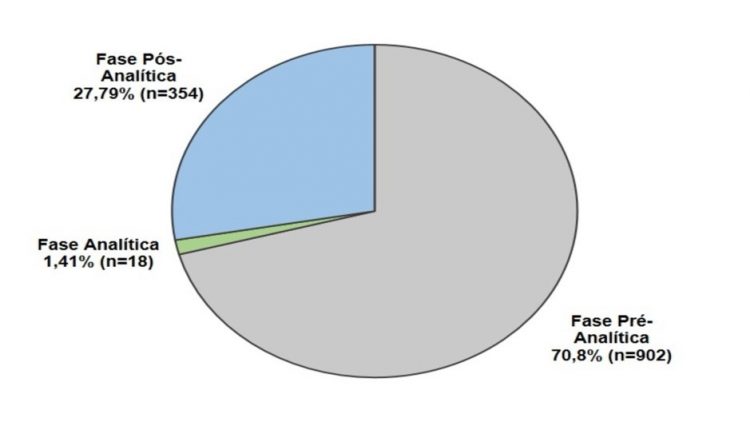
Figura 2
Comparação entre as fases de realização de exames em relação às taxas de novas ordens de coleta.
Fonte: Adaptado de Fernandes e Oliveira, 2016(6)
Tabela 1
Erros pré-analíticos por Ashakiran et al. (2011) após três meses de estudo
| Erros pré-analíticos | Frequência de Dez/2009 a Fev/2010 (n) |
| Erros que ocorrem no nível de identificação do paciente | |
| Solicitação inadequada | 28,8 (51) |
| Identificação incorreta | 2,8 (5) |
| Erros que ocorrem no nível da coleta da amostra | |
| Tempo inadequado da amostra | 20,9 (37) |
| Amostra insuficiente | 7,3 (13) |
| Coleta inadequada de tubos | 15,3 (27) |
| Erros que ocorrem durante o transporte da amostra | |
| Atraso no manuseio e transporte da amostra | 5,6 (10) |
| Hemólise in vitro | 19,2 (34) |
| Total | 100 (177) |
Fonte: Ashakiran et al., 2011(15)
Tabela 2
Erros pré-analíticos por Guimarães et al. (2012) após três meses de estudo
| Erros pré-analíticos | Frequência de Jun/2010
a Ago/2010 (n) |
| Amostra coagulada | 43,8 (193) |
| Volume insuficiente de amostra | 24 (106) |
| Amostra hemolisada | 17,9 (79) |
| Erro na identificação da amostra | 4,3 (19) |
| Erro na escolha do tubo/aditivo | 1,8 (8) |
| Amostra lipêmica | 0.9 (4) |
| Razão amostra/aditivo inadequado | 0,7 (3) |
| Amostra com icterícia | 0,7 (3) |
| Outras causas de rejeição | 5,9 (26) |
| Total | 100 (441) |
Fonte: Guimarães et al., 2012(16)
Corroborando as informações já mencionadas, Fernandes e Oliveira(6) demonstraram em seu estudo, realizado em um laboratório de análises clínicas na cidade de Maringá-PR, Brasil, em que os dados foram obtidos através do relatório de coleta de dados do controle de qualidade e dos formulários de não conformidades do próprio laboratório, que do total de 707.449 testes realizados em amostras de pacientes 1.274 testes obtiveram uma nova ordem de coleta por estarem impróprios para a realização de exames, 902 (70,8%) destas amostras haviam sido rejeitadas em virtude de erros cometidos na fase pré-analítica. O volume insuficiente de amostra, amostra coagulada e amostra hemolisada foram os erros que se destacaram neste estudo, como mostra a Tabela 3.(6)
Tabela 3
Erros pré-analíticos por Fernandes e Oliveira (2016) após dois anos de estudo
| Erros pré-analíticos | Frequência de Jun/2013 a Mai/2015 (n) |
| Amostra coagulada | 19,29 (174) |
| Amostra hemolisada | 9,43 (85) |
| Amostra lipêmica | 3 (27) |
| Rotulagem incorreta da amostra | 8,21 (74) |
| Amostra inadequada | 1,56 (14) |
| Volume insuficiente da amostra | 58,54 (528) |
| Total | 100 (902) |
Fonte: Fernandes e Oliveira, 2016(6)
Durante o período de realização de um estudo executado por Tapper et al. (2017),(17) após avaliar os erros pré-analíticos encontrados no registro de rejeição de amostras do laboratório observou-se que 1.390 amostras foram rejeitadas devido a erros provocados na fase pré-analítica, porém as informações sobre o número total de amostras recebidas pelo laboratório não foram relatadas. Amostras não identificadas, amostras rotuladas incorretamente, tubos inadequados de coleta para o teste solicitado, assim como o preenchimento incompleto ou impreciso do formulário de requisição representaram a maioria dos erros pré-analíticos registrados, como demonstrado na Tabela 4.(17)
Um estudo elaborado recentemente por Kadić et al.(18) analisou os dados de amostras de sangue rejeitadas de acordo com os registros do sistema de informação laboratorial, demonstrando que do total de 35.343 amostras, 602 (1,70%) foram rejeitadas por erros cometidos na fase pré-analítica. Os erros que apresentaram uma maior frequência foram amostras hemolisadas, amostras coaguladas e volume inadequado de amostra, conforme mostra a Tabela 5.(18)
Tabela 4
Erros pré-analíticos por Tapper et al. (2017) após quatro anos de estudo
| Erros pré-analíticos | Frequência de Jun/2012 a Mai/2016 (n) |
| Amostra Inadequada | |
| Rotulagem incorreta da amostra | 23 (326) |
| Não etiquetada | 37 (513) |
| Amostra hemolisada | 3,3 (46) |
| Amostra inadequada para análise | 2,0 (29) |
| Amostra antiga | 0,2 (4) |
| Formulário de requisição inadequado | |
| Informações incompletas/imprecisas | 14 (194) |
| Nenhum teste solicitado | 0,3 (5) |
| Manchado de sangue | 0,5 (7) |
| Volume inadequado | |
| Amostra vazada em trânsito | 0,9 (13) |
| Amostra quebrada em trânsito | 1,0 (14) |
| Nenhuma amostra recebida | 0,5 (8) |
| Quantidade insuficiente | 1,2 (18) |
| Amostra quebrada/derramada em laboratório | 1,3 (19) |
| Tubo inadequado | |
| Amostra incorreta para teste | 14 (194) |
| Total | 100 (1.390) |
Fonte: Tapper et al., 2017(17)
E por fim, Dhotre et al.(19) atualmente desenvolveram um estudo em um período de 12 meses, contendo duas fases de pesquisa: uma antes do treinamento da equipe de flebotomistas do laboratório e a outra após o treinamento, contendo seis meses cada fase.(19)
De acordo com os autores, amostras foram rejeitadas pela equipe do laboratório de acordo com os seus procedimentos operacionais padrão, que foram devidamente anotados no livro de registro de amostras rejeitadas, onde obteve um total de 980 erros pré-analíticos, dos quais 740 erros ocorreram na primeira fase do estudo e 240 erros na segunda fase. O número total de amostras recebidas pelo laboratório não foi relatado pelo autor. Amostra hemolisada, amostra lipêmica e quantidade de amostra insuficiente estão entre os erros que mais se destacaram, de acordo com a Tabela 6, que mostra os resultados baseados na primeira fase do estudo.(19)
Na segunda fase do estudo foram observados os mesmos erros descritos na primeira fase (Tabela 6), porém não houve diferença significativa nas proporções dos diferentes tipos de erros entre as duas fases do estudo.(19)
Desta forma, o presente trabalho reuniu os principais erros pré-analíticos com base nos registros dos estudos aqui citados, a partir de uma análise feita em seus dados. A Tabela 7 apresenta os percentuais dos erros pré-analíticos mais frequentes entre os estudos avaliados, ou seja, aqueles relatados em pelo menos 50% destes.
A Figura 3 nos mostra a distribuição da frequência dos erros pré-analíticos conforme os dados da Tabela 7, fazendo uma comparação da porcentagem destes erros encontrados em cada estudo com outra perspectiva.
Nota-se que os erros referentes a volume inadequado de amostra, amostra hemolisada e amostra coagulada atingiram uma maior taxa quando comparados aos demais erros. De todos os outros erros pré-analíticos que foram relatados nos seis estudos, a amostra hemolisada se destacou em cinco estudos por estar entre os que atingiram as maiores porcentagens de erros pré-analíticos, assim como o volume inadequado de amostra que se destacou em quatro estudos, e a amostra coagulada que também se evidenciou em três estudos.(6,15,16,18,19)
Em suma, os resultados laboratoriais precisos são essenciais para o diagnóstico médico e atendimento ao paciente, visto que grande parte dos diagnósticos é concluída com base nos resultados dos exames. No entanto, mediante o exposto em relação às altas taxas de erros pré-analíticos que são encontrados até os dias atuais, a grande questão é: até que ponto esses erros podem impactar os resultados dos exames laboratoriais e, consequentemente, a saúde do paciente?(19)
Tabela 5
Erros pré-analíticos por Kadić et al. (2019) após três meses de estudo
| Erros pré-analíticos | Frequência de Dez/2016
a Mar/2017 (n) |
| Hemólise | 48,50 (292) |
| Amostra coagulada | 39,87 (240) |
| Volume de amostra inadequado | 7,81 (47) |
| Tubo de coleta inadequado | 2,16 (13) |
| Erro de identificação | 1,66 (10) |
| Total | 100 (602) |
Fonte: Kadić et al., 2019(18)
Tabela 6
Erros pré-analíticos por Dhotre et al. (2020) após seis meses de estudo
| Erros pré-analíticos | Frequência de Jan/2019
a Jun/2019 (n) |
| Amostras hemolisadas | 36,6 (271) |
| Amostras lipêmicas | 19,9 (147) |
| Quantidade inadequada de amostra | 18,8 (139) |
| Atraso no transporte da amostra | 13,4 (99) |
| Coleta de amostra em tubo errado | 11,4 (84) |
| Total | 740 (100) |
Fonte: Dhotre et al., 2020(19)
Tabela 7
Erros pré-analíticos com maior reincidência entre os estudos
| Autor/ano | ASHAKIRAN, SUMATI & MURTHY, 2011 | GUIMARÃES et al., 2012 | FERNANDES & OLIVEIRA, 2016 | TAPPER et al., 2017 | KADIĆ, AVDAGIĆ-ISMIĆ & HASIĆ, 2019 | DHOTRE, DHOTRE & SHAIKH, 2020 |
| Período de obtenção dos dados | 3 meses | 3 meses | 2 anos | 4 anos | 3 meses | 6 meses |
| Erros pré-analíticos
Frequência (%) |
||||||
| Identificação incorreta da amostra | 2,8 | 4,3 | 8,21 | 23 | 1,66 | * |
| Volume inadequado de amostra | 7,3 | 24 | 58,54 | 5,1 | 7,81 | 18,8 |
| Amostra hemolisada | 19,2 | 17,9 | 9,43 | 3,3 | 48,50 | 36,6 |
| Tubo de coleta inadequado | 15,3 | 1,8 | * | 14 | 2,16 | 11,4 |
| Amostra coagulada | * | 43,8 | 19,29 | * | 39,87 | * |
| Amostra lipêmica | * | 0,9 | 3 | * | * | 19,9 |
Legenda:(*) representa a ausência do erro pré-analítico no estudo.
Fonte: Ashakiran et al., 2011(15); Guimarães et al., 2012(16); Fernandes e Oliveira, 2016(6); Tapper et al., 2017(17); Kadić et al., 2019(18); Dhotre et al., 2020(19)
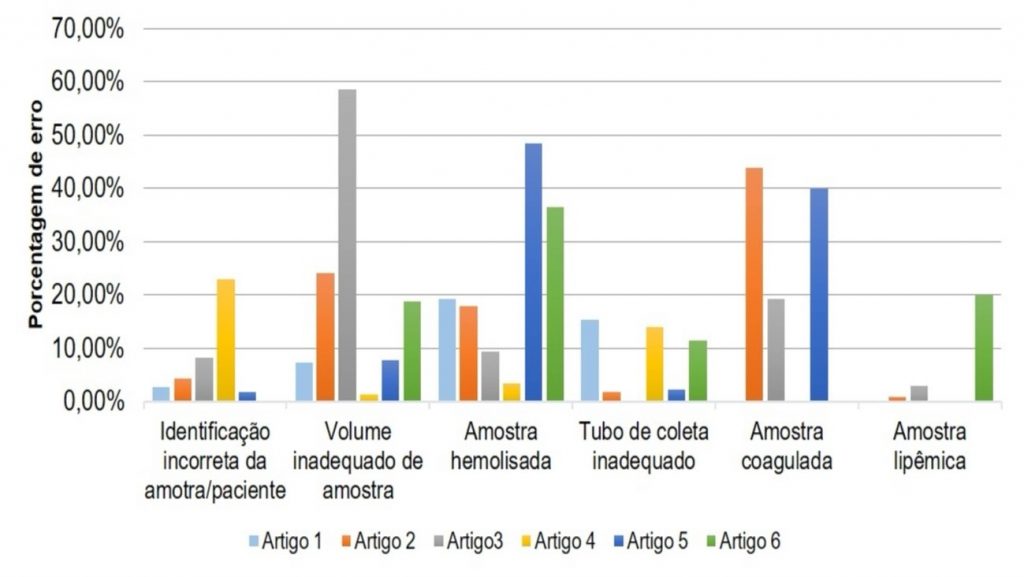
Figura 3
Porcentagem dos principais erros pré-analíticos
Legenda: Artigo 1 – Ashakiran et al. (2011); Artigo 2 – Guimarães et al. (2012); Artigo 3 – Fernandes e Oliveira (2016); Artigo 4 – Tapper et al. (2017); Artigo 5 – Kadić et al. (2019); Artigo 6 – Dhotre et al. (2020).
Fonte: Ashakiran et al., 2011(15); Guimarães et al., 2012(16); Fernandes e Oliveira, 2016(6); Tapper et al., 2017(17); Kadić et al., 2019(18); Dhotre et al., 2020(19)
DISCUSSÃO
O estudo de Salinas et al.(20) afirma que é na fase pré-analítica que se concentra o maior percentual de erros relacionados aos exames laboratoriais. O autor também aponta que em diferentes trabalhos as frequências desses erros podem atingir entre 31,6%, 44% e 53%, podendo chegar até 75%, onde esses dados se mostram compatíveis com os números relatados no presente estudo. Segundo o autor, estas distinções se dão por causa dos diferentes critérios de avaliação ou pelo aumento das variáveis do estudo.(20)
Vieira et al.(11) também fazem uma comparação em relação às porcentagens de erros entres as três fases de realização das análises clínicas laboratoriais, e apontam que de 46% a 68% dos erros estão relacionados à fase pré-analítica, 12,5% dos erros estão ligados à fase analítica e que, por fim, de 18% a 47% dos erros são provocados na fase pós-analítica, similarmente com os dados apresentados na Figura 1 e na Figura 2.(11)
Porém as taxas dos erros pré-analíticos apresentam variações quando comparadas entre os estudos que foram mencionados. Segundo Lee (2019),(21) comparar os tipos e frequências de erros pré-analíticos entre laboratórios ou entre países é bem difícil, por causa dos diferentes ambientes e sistemas de saúde, serviços prestados pelo laboratório, podendo também estar relacionado à forma como estes erros foram detectados, pois segundo o autor não é fácil identificar os erros pré-analíticos com precisão porque também é difícil contar com o compromisso dos laboratórios em registrar estes erros.(21)
Grande parte dos erros laboratoriais, quando identificados, irá resultar na rejeição das amostras biológicas e, consequentemente, em uma nova coleta de amostra. Segundo Guimarães et al.(8), este fato pode provocar insatisfação, transtornos, ansiedade e inseguranças ao médico e ao paciente. Já em relação ao âmbito laboratorial, estes erros provocam custos desnecessários, atrasos na liberação dos resultados, aumento da carga de trabalho e, principalmente, a perda da credibilidade, confiança e segurança no laboratório, provocando um efeito negativo em sua imagem.(8)
Diversos estudos mostram que estão entre os tipos de erros pré-analíticos mais comumente relatados a identificação incorreta da amostra/paciente, volume inadequado de amostra, amostra hemolisada, tubo de coleta inadequado, amostra coagulada e amostra lipêmica, corroborando com os principais erros pré-analíticos encontrados no presente estudo (Tabela 7).(2,7,11,22,23)
O estudo de Green(2) relatou que a identificação incorreta estava entre uma das causas mais frequentes de erros pré-analíticos. Sushma e Shrikant(7) afirmam que a identificação do paciente é a principal etapa crítica na coleta de sangue. Segundo estes autores, este erro provavelmente pode ser provocado devido à grande carga de trabalho. Realizar a punção venosa da pessoa errada ou rotular erroneamente a amostra biológica de um paciente pode contribuir para o erro laboratorial, isto porque, segundo Green(2), este incidente pode resultar em diagnóstico tardio, testes laboratoriais extras, tratamento inadequado, podendo até mesmo ser fatal se resultar em uma reação hemolítica aguda em casos de transfusão de sangue.(2,7)
Para reduzir este erro laboratorial relacionado à identificação, Sushma e Shrikant(7) preconizam que ao identificar o paciente, informações como nome completo, endereço, número de identificação e/ou data de nascimento devem ser confirmadas. Além disso, pacientes hospitalizados devem utilizar identificação com as informações descritas anteriormente, para que antes da punção venosa o flebotomista possa confirmar esses dados e verificar se a faixa ou pulseira de identificação está presa ao paciente. Pulseiras de identificação com código de barras possuem grande potencial para a redução deste erro. Os flebotomistas devem se apresentar de forma agradável e explicar ao paciente o procedimento que será realizado. Também é necessário que o paciente diga o seu nome; caso isto não seja possível, ele deverá fornecer alguma forma de identificação ou ser identificado por algum membro da família ou cuidador.(7)
No estudo de Codagnone et al.(24), o volume insuficiente de amostra foi a terceira causa dos erros pré-analíticos que foram identificados. De acordo com Green(2), a quantidade insuficiente de amostra é problemática, já que em alguns casos nem todos os testes solicitados pelo médico poderão ser realizados, o que irá exigir uma nova coleta, e com isso atrasos nos resultados dos exames e novos gastos.(2)
Os tubos de coleta devem ser preenchidos com volume correto de amostra para garantir a proporção sangue/aditivo, pois, por exemplo, quantidade insuficiente de amostra em tubos de heparina pode resultar na elevada concentração de heparina e, consequentemente, interferir nos resultados de alguns analitos.(2) Um outro exemplo é dado por Magnette et al.(25), em que os autores relatam que tubos de citrato de sódio devem ser enchidos até 90% do seu volume ou até a marca anotada no tubo, pois em casos de volume insuficiente de amostra ocorre o aumento de sua diluição em razão do volume do anticoagulante líquido e pode aumentar o tempo de coagulação por causa do excesso de citrato ligante de cálcio presente no tubo de coleta.(25)
Os autores Codagnone et al.(24), Marín et al.(23) e Sushma e Shrikant(7) apontaram que a principal causa de erro pré-analítico em seus estudos foi a hemólise.(7,23,24) Segundo Green(2), a presença de hemólise é responsável por 40% a 70% das amostras biológicas inadequadas que chegam ao seu laboratório. Este autor afirma que esse erro pré-analítico pode ser causado pela mistura vigorosa da amostra de sangue, pelo transporte pneumático das amostras feito pelo tubo ou por forçar o sangue através da agulha.(2)
Para Codagnone et al.(24), alguns fatores também podem influenciar a ocorrência de hemólise como a aplicação prolongada do torniquete, constrição inadequada dos músculos do antebraço e seleção inadequada do calibre da agulha para a coleta venosa.(24) Marín et al.(23) relatam que os motivos deste erro pré-analítico podem estar relacionados à pouca utilização de tubos a vácuo, de maneira que os tubos de amostras são preenchidos diretamente com a seringa; além disso, acrescentam que os funcionários não são suficientemente qualificados para o processo de coleta.(23)
A ruptura das hemácias que resulta na hemólise, mesmo que em um grau leve, pode influenciar os resultados de exames de vários analitos, como LDH, CK, K, AST, ALT, ACP, ALP, ALB, Cl, GGT, GLI, CRE e Na. De fato, quando a amostra está hemolisada, parâmetros como K, ALT, CRE e CK estão superestimados, enquanto parâmetros como ALB, ALP, CL, GGT, GLI e Na estão subestimados.(2,7,24)
Segundo Magnette et al.,(25) para evitar a ocorrência de hemólise em amostras de sangue venoso, algumas medidas devem ser tomadas. Dentre elas podemos citar: aplicação de torniquete em menos de 1 minuto e a obtenção das amostras sem a provocação de traumas, onde o sangue deve fluir livremente para o tubo de coleta sem gerar espuma ou bolhas na amostra e com a mínima tensão. Além disso, também é descrito na literatura sobre a importância da utilização de coletas a vácuo, pois a transferência direta de amostra da seringa para o tubo faz com que as células colidam com a parede do tubo sob a pressão do êmbolo. Ademais, a agitação vigorosa do sangue deve ser evitada e deve haver seleção adequada dos dispositivos de coleta.(25)
Guimarães et al.(8), Costa e Moreli(13) e Marín et al.(23) revelam que tubos de coleta de amostra inadequados estão entre os erros pré-analíticos que foram identificados em seus respectivos estudos.(8,13,23) O estudo de Grecu et al.(26) afirma que amostras tem sido coletadas em tubos com anticoagulantes inadequados.(26) Segundo Li et al., este erro pré-analítico pode estar associado ao descuido das equipes de coleta.(27)
Segundo Najat(28), um dos erros pré-analíticos que atingiram maior porcentagem em seu estudo foi a amostra coagulada.(28) De acordo com Magnette et al.(25), uso prolongado do torniquete, manipulação considerável da agulha na veia, não homogeneização da amostra em tubo contendo anticoagulante ou feita de forma errada, podem provocar a formação de coágulo na amostra.(25) Green(2) relata em seu estudo que a coagulação da amostra pode produzir falsa leucopenia, baixa contagem de hemácias, além da diminuição dos valores de hematócrito. Além disso, os microcoágulos podem ser aspirados e levar à obstrução da sonda dos aparelhos.(2)
Os estudos de Sushma e Shrikant(7) e Sua et al.(4) revelaram que amostra lipêmica foi um dos erros pré-analíticos detectados em seus respectivos estudos.(4,7) O autor Nikolac(29) afirma que a lipidemia é a presença de turvação na amostra de sangue, causada pelo acúmulo de partículas de lipoproteína. Ele também relata que a causa pré-analítica mais comum de lipidemia é o tempo inadequado da coleta de sangue, ou seja, após a refeição. O correto é que os pacientes estejam devidamente preparados e em jejum (que pode variar entre quatro a doze horas de jejum após a última refeição) antes da coleta de sangue. Segundo o autor, isso ocorre porque os pacientes não são devidamente informados sobre como deve proceder o preparo para a coleta de sangue.(29)
O plasma sanguíneo normal consiste em aproximadamente 92% de água e 8% de lipídios, porém na amostra lipêmica a proporção da fase lipídica aumenta e pode chegar a 25%. Desta forma, a lipidemia pode interferir nos resultados dos testes que utilizam métodos de espectrofotometria, já que partículas de lipoproteínas na amostra podem absorver a luz. A quantidade de luz absorvida é inversamente proporcional ao cumprimento de onda, portanto métodos que utilizam cumprimentos de onda menores são mais afetados, pois a absorbância é maior, e sendo assim a lipidemia pode afetar os resultados de alguns parâmetros bioquímicos como ALT, AST e GLI.(7,29)
Segundo Guimarães et al.,(8) erros pré-analíticos estão geralmente associados à elevada rotatividade de pessoas, falta de entendimento sobre as boas práticas laboratoriais, negligência e à falta de capacitação e treinamento dos profissionais envolvidos nos processos pré-analíticos.(8) Os estudos de Marín et al.(23) e Lee(21) afirmam que os erros pré-analíticos estão diretamente ligados ao processo de coleta de sangue, corroborando as informações obtidas neste estudo, já que grande parte dos erros pré-analíticos encontrados estão relacionados a falhas provocadas durante a punção venosa.(21,23)
De acordo com os estudos de Li et al.,(27) Lee(21) e Dhotre et al.,(19) o treinamento e capacitação da equipe de flebotomia gerou melhorias significativas, de forma que estes obtiveram aprimoramento das técnicas de coletas de amostras, que resultou na redução das taxas de erros pré-analíticos.(19,21,27)
CONCLUSÃO
Esta revisão bibliográfica conclui que, apesar dos avanços tecnológicos, a fase pré-analítica ainda é a principal responsável pelos erros laboratoriais e que a maior parte dos erros pré-analíticos estão enraizados nos setores de coleta sanguínea. Cada um dos erros apontados neste estudo possui grande potencial para afetar de diversas formas a qualidade dos resultados e dos testes laboratoriais. Uma pequena falha no processo de coleta sanguínea pode gerar danos ao laboratório e principalmente à saúde do paciente.
Portanto, recomenda-se a realização de treinamentos periódicos e a implantação de programas de educação continuada voltadas para as equipes de flebotomia (envolvendo palestras, aplicação de questionários para avaliar e nivelar o grau de conhecimento destas equipes), focados nas técnicas de punção venosa, ordem e escolha correta dos tubos e dos materiais que serão usados na coleta, utilização de etiquetas com código de barras, preparação adequada do paciente e aplicação dos critérios de rejeição de amostras.
Com isso, estas medidas possuem o objetivo de proporcionar um aperfeiçoamento destes processos e, consequentemente, reduzir as taxas dos erros pré-analíticos, gerando a melhoria do atendimento ao paciente e a emissão de resultados mais fidedignos.
SUPORTE FINANCEIRO
A pesquisa não recebeu financiamento para sua realização.
REFERÊNCIAS
- Fernandes JLN, Wollinger W, Garrido BC. Rastreabilidade em medicina laboratorial: um estímulo global para resultados exatos no cuidado com o paciente. J Bras Patol Med Lab. 2019; 55(4):402-411.
- Green SF. The cost of poor blood specimen quality and errors in preanalytical processes. Clin Biochem. 2013; 46(13-14):1175-1179.
- Aragão DP, Araujo RML. Orientação ao paciente antes da realização de exames laboratoriais. Rev Bras Anal Clin. 2019; 98-102.
- Sua LF, Amezquita MA, Hernández DE, Alcalá-Flores M, Leib CS, Aguirre-Rojas M, et al. Estaciones automatizadas preanalíticas en el laboratorio de hemostasia. Estudio observacional descriptivo prospectivo, realizado en un hospital universitario de referencia entre el 15 de abril y 15 de julio de 2017. Iatreia. 2019; 32(3):177-183.
- Faria GM, Pereira RL, Lourenço PM. Erros pré-analíticos em medicina laboratorial: uma avaliação preliminar em diferentes laboratórios de análises clínicas. Rev Bras Anal Clin. 2015; 47(3):105-109.
- Fernandes TRL, Oliveira CF. Analysis of the pre-analytical phase in a private pathology laboratory of Maringá city-PR, Brazil. J Bras Patol Med Lab. 2016; 52(2):78-83.
- Sushma BJ, Shrikant C. Study on “Pre-analytical Errors in a Clinical Biochemistry Laboratory”: The Hidden Flaws in Total Testing. Anal Biochem. 2019; 8(374):2161-1009.19.
- Guimarães AC, Wolfart M, Brisolara MLL, Dan C. O laboratório clínico e os erros pré-analíticos. Rev HCPA. 2011; 31(1):66-72.
- Ambachew S, Adane K, Worede A, Melak T, Asmelash D, Damtie S, et al. Errors in the total testing process in the clinical chemistry laboratory at the University of Gondar Hospital, Northwest Ethiopia.Ethiop J Health Sci. 2018; 28(2):235-244.
- Martins JM, Rateke ECM, Martinello F. Assessment of the pre-analytical phase of a clinical analyses laboratory. J Bras Patol Med Lab. 2018; 54(4):232-240.
- Vieira KF, Shitara ES, Mendes ME, Sumita NM. A utilidade dos indicadores da qualidade no gerenciamento de laboratórios clínicos. J Bras Patol Med Lab. 2011; 47(3):201-210.
- Ramos LR, Oliveira MV, Souza CL. Avaliação de variáveis pré-analíticas em exames laboratoriais de pacientes atendidos no Laboratório Central de Vitória da Conquista, Bahia, Brasil. J Bras Patol Med Lab. 2020; 56: 1-8.
- Costa VG, Moreli ML. Principais parâmetros biológicos avaliados em erros na fase pré-analítica de laboratórios clínicos: revisão sistemática. J Bras Patol Med Lab.2012; 48(3):163-168.
- Campana GA, Oplustil CP, Faro LB. Tendências em medicina laboratorial. J Bras Patol Med Lab. 2011; 47(4):399-408.
- Ashakiran S, Sumati ME, Murthy NK. A study of pre-analytical variables in clinical biochemistry laboratory. Clin biochem.2011; 44(10-11):944-945.
- Guimarães AC, Wolfart M, Brisolara ML, Dani C. Causes of rejection of blood samples handled in the clinical laboratory of a University Hospital in Porto Alegre. Clin Biochem. 2012; 45(1-2):123-126.
- Tapper MA, Pethick JC, Dilworth LL, McGrowder DA. Pre-analytical errors at the chemical pathology laboratory of a teaching hospital. JCDR. 2017; 11(8):BC16.
- Kadić D, Avdagić-ismić A, Hasić S. The prevalence of pre-analytical errors in the laboratory of the Cantonal Hospital Zenica in Bosnia and Herzegovina. Med Glas. 2019; 16(1).
- Dhotre PS, Dhotre SV, Shaikh A. A Comparative Study of Pre-analytical Errors in Central Clinical Laboratory in a Tertiary Care Hospital in Maharashtra. JKIMSU. 2020; 9(2).
- Salinas M, López-Garrigós M, Yago M, Ortuño M, Carratala A, Aguado C, et al. Evaluación de la calidad en el laboratorio en la fase preanalítica: un estudio multicéntrico. Rev Calid Asist. 2011; 26(4):264-268.
- Lee NY. Reduction of pre-analytical errors in the clinical laboratory at the University Hospital of Korea through quality improvement activities. Clin Biochem. 2019;70: 24-29.
- Plebani M. Quality indicators to detect pre-analytical errors in laboratory testing. Clin Biochem Rev. 2012; 33(3):85.
- Marín AG, Ruiz FR, Hidalgo MMP, Mendoza PM. Pre-analytical errors management in the clinical laboratory: a five-year study. Biochem Med. 2014; 24(2):248-257.
- Codagnone FT, Alencar SMF, Shcolnik W, Chaves SRDS, Silva LA, Henriques VHO. The use of indicators in the pre-analytical phase as a laboratory management tool. J Bras Patol Med Lab. 2014;50(2):100-104.
- Magnette A, Chatelain M, Chatelain B, Ten Cate H, Mullier F. Pre-analytical issues in the haemostasis laboratory: guidance for the clinical laboratories. Thromb j.2016; 14(1):49.
- Grecu DS, Vlad DC, Dumitrascu V. Quality indicators in the preanalytical phase of testing in a stat laboratory. Lab Med. 2014; 45(1):74-81.
- Li HY, Huang XN, Yang YC, Huang WF, Chen L, Song P, et al. Reduction of preanalytical errors in clinical laboratory through multiple aspects and whole course intervention measures. J Evid Based Med. 2014; 7(3):172-177.
- Najat D. Prevalence of pre-analytical errors in clinical chemistry diagnostic labs in Sulaimani city of Iraqi Kurdistan. PLos ONE. 2017; 12(1):e0170211.
- Nikolac N. Lipemia: causes, interference mechanisms, detection and management. Biochem Med. 2014; 24(1):57-67.
Correspondência
Giselle Aparecida Fagundes Silva
Universidade do Grande Rio
Rua Prof. José de Souza Herdy, 1.160 – Jardim 25 de Agosto
Duque de Caxias – Rio de Janeiro
E-mail: [email protected]
